近日,意昂4体育平台古宏晨-徐宏研究團隊在新型超高通量懸浮芯片的設計構建及用於單反應多指標生物檢測技術方面取得突破性進展,研究成果“Precisely Encoded Barcodes through the Structure-Fluorescence Combinational Strategy: A Flexible, Robust, and Versatile Multiplexed Biodetection Platform with Ultrahigh Encoding Capacities”以封面論文發表在微納米材料領域權威期刊《Small》上😳🚾。

隨著人類對生命現象認識的深入,利用多種生物標誌物的組合可以對疾病的發生、發展及預後進行更加精準的檢測、診斷以及治療指導👩🏿🚒。懸浮芯片以其靈敏而準確的光學編碼鑒別、快速的反應動力學🪒、靈活的檢測項目組合、可實現定量分析以及同時適用於蛋白與核酸分子檢測等特點而成為最理想的多重指標聯合檢測的技術平臺,並被列入“十三五”國家科技創新規劃。編碼微球是懸浮芯片技術的核心,也是中國體外診斷領域中上遊核心原材料所面臨的“卡脖子技術”之一。但目前國際上主流的基於多色熒光染料的編碼策略存在染料分子間相互幹擾從而影響編碼的準確性與可控性,同時該策略對微球基質的選擇亦不靈活,使得懸浮芯片在面臨超高通量多指標檢測時仍有較大挑戰。
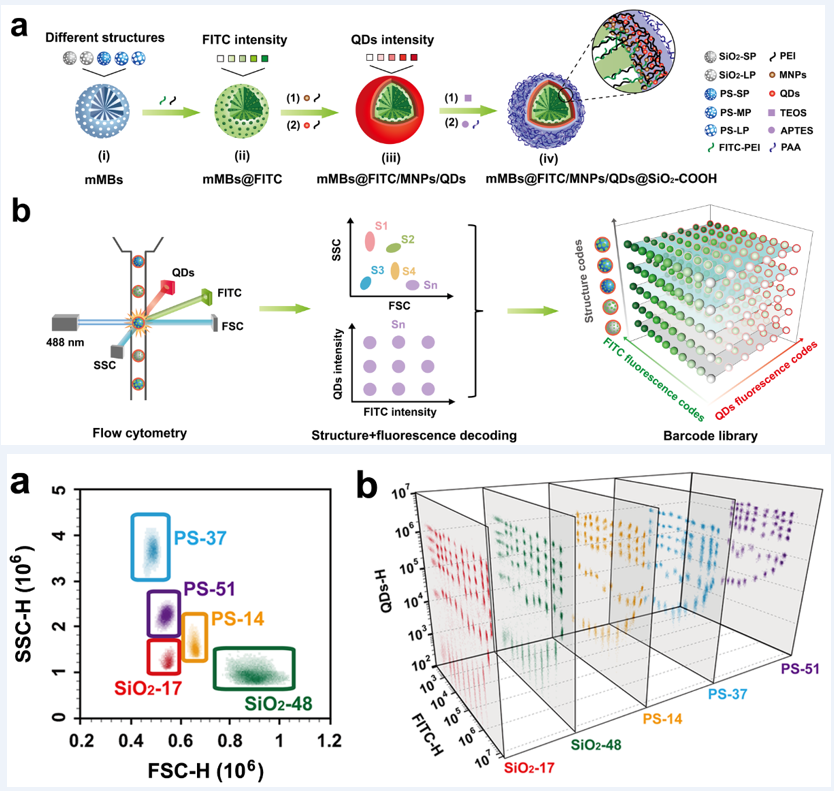
為解決本領域的上述重要問題,該團隊在國際上首次發現了通過改變介孔微球的孔隙率和基質成分等微球內部的精密結構👧🏽,可在流式細胞儀上產生特殊的散射光信息,每類微球獨特且有規律的散射光信息具有分群特征,從而提出了微球結構可作為一種全新維度的光學編碼元素的假設。在此基礎上,研究者創新性地提出了“結構-熒光”聯合編碼策略,即通過發展可對無機和有機微球均具有普適性的聚合物介導的染料摻雜法(該方法近期發表在Chem. Commun., 2021, DOI: 10.1039/d0cc08202c)在介孔微球的孔道內裝載熒光染料分子,再在微球的外表面利用層層自組裝法依次裝載磁性納米顆粒和熒光量子點納米晶,成功建立了集三種編碼元素(結構和雙色熒光)、以及超順磁特性的超高通量懸浮芯片系統👨🏿🏭。再利用流式細胞儀作為解碼系統,成功實現了單色激光在單個反應管中一次激發與鑒別出300重編碼微球🐫,這是目前已有報道的最高記錄🧑⚖️,取得了本領域的突破🍎。同時🤹🏽♂️,利用該懸浮芯片系統還進一步實現了單管10重腫瘤標誌物的聯合檢測👱,展現了多重指標聯合檢測的實際應用潛力🪨。相關研究成果發表於《Small》(2021, 17, 2100315.),論文的第一作者為青年教師王耀助理研究員🚘,通訊作者為徐宏研究員。此工作還得到了意昂4体育平台葉堅教授🥒、鄔崇朝長聘教軌副教授等團隊的大力支持♤。該研究得到了國家自然科學基金(重大儀器專項、面上項目🧔🏿♂️、青年項目)、上海市自然科學基金、上海市高峰高原學科建設🐡、意昂4平台醫工交叉等基金項目的資助🎅🏽。
上述研究成果是古宏晨教授和徐宏研究員領導的科研大團隊在高通量懸浮芯片及多指標生物檢測領域取得的又一創新性突破。該團隊近年來已陸續發展了四代具有不同精密微納結構的懸浮芯片系統,並在微納米材料領域權威期刊上連續以封面論文的形式進行報道,包括第一代主-客體組裝結構的二維熒光編碼平臺(Adv. Funct. Mater., 2016, 26, 6146.)、第二代具有主-客體結構的尺寸-熒光聯合的三維編碼技術(Chem. Mater., 2017, 29, 10398.)、第三代基於光激化學發光的多重檢測免洗式懸浮芯片(Small, 2020, 16, 1907521.)⏯、以及此次報道的第四代基於分區設計的結構-熒光聯合編碼技術(Small, 2021, 17, 2100315.),在本領域產生了持續性的重要影響力。
論文鏈接:
1. Y. Wang, C. Chen, J. He, Y. Cao, X. Fang, X. Chi, J. Yi, J. Wu, Q. Guo, H. Masoomi, C. Wu, J. Ye, H. Gu, H. Xu*. Small, 2021, 17, 2100315.
https://doi.org/10.1002/smll.202100315
2. H. Masoomi#, Y. Wang#,*, C. Chen, J. Zhang, Y. Ge, Q. Guo, H. Gu, H. Xu*. Chem. Commun., 2021, 57, 4548.
https://pubs.rsc.org/en/content/articlelanding/2021/cc/d0cc08202c#!divAbstract